新冠病毒的遗传进化之路
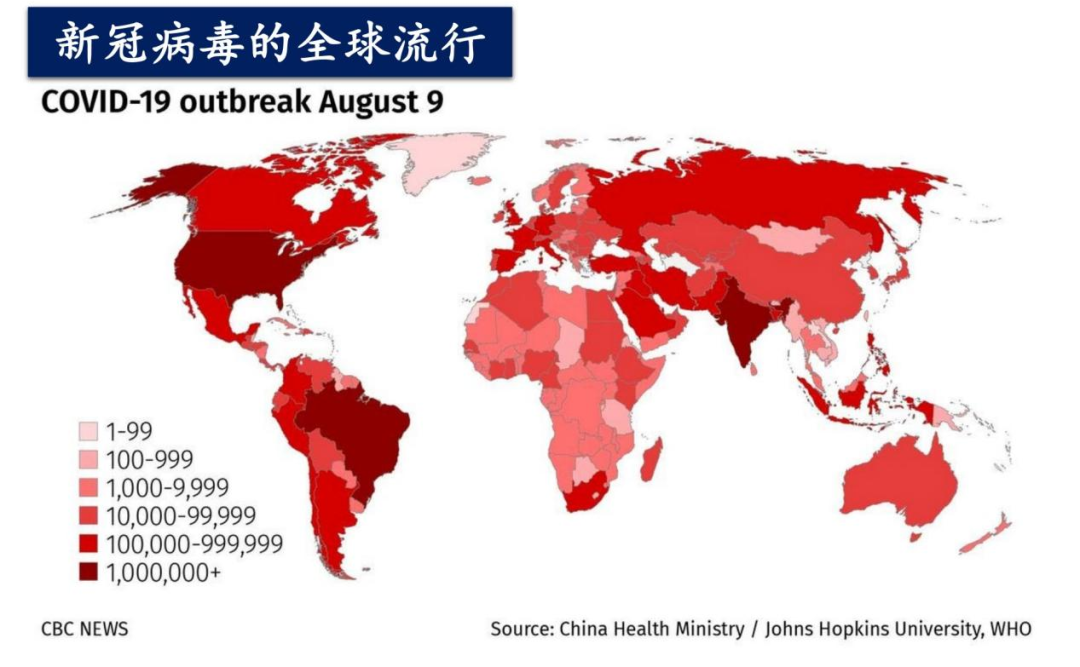
新冠病毒从2019年末开始流行肆虐至今,持续了3年时间,已经造成4.5亿人次感染,超600万死亡病例,纵观人类历史,除了少数几次病毒大流行以外,很少有一场疫情可以持续如此长的时间。近期在深圳市局部流行的新冠病毒为最新的奥密克戎变异株,其具有传播力强、传播速度快、隐匿性高、人群普遍易感等特点,给疫情防控工作带来更为严峻挑战。
新冠病毒经历了怎样的遗传进化之路?它是如何不断进化突变,来维系自身在宿主间的高效传播?疫苗接种作为防控病毒传染病最普适性的手段,不同种类疫苗有何优缺点?如何接种才能高效避免感染?
近日深圳湾实验室特聘研究员刘洋在Bioart与一作面对面论坛分享题为“新冠病毒变种和疫苗接种”的报告,以下为演讲实录第一部分:
近年来,全球范围内各类传染病疫情不断暴发,严重威胁国民健康。这些传染病的病原体多为高致病性、高重症率、高致死率的病毒,比如登革病毒、寨卡病毒、黄热病毒、埃博拉病毒、MERS和SARS-CoV-2。它们的流行造成了数以亿计的感染和数百万人的死亡。WHO最新公布的8种最需要关注的传染病也均由病毒传播,包括了2种呼吸道传播病毒MERS和SARS-CoV-2,3种虫媒传播病毒克里米亚刚果出血热,裂谷热和寨卡;两种通过密切接触传播的尼帕病毒和拉沙热病毒,以及感染能力极强的直接接触传播的埃博拉病毒。可以预见,在未来的数十年里,病毒类传染病将会成为,对人们健康的最重大威胁之一。
新冠病毒从2019年末开始流行,并肆虐至今,持续了3年时间,已经造成4.5亿人次感染,超600万死亡病例;各类突变病毒毒株层出不穷,对人们健康造成了极大威胁。纵观人类历史,除了少数几次病毒大流行以外,很少有一场疫情可以持续如此长的时间。新冠病毒在流行的过程中,不断的适应人类宿主,增强自身的感染和传播。
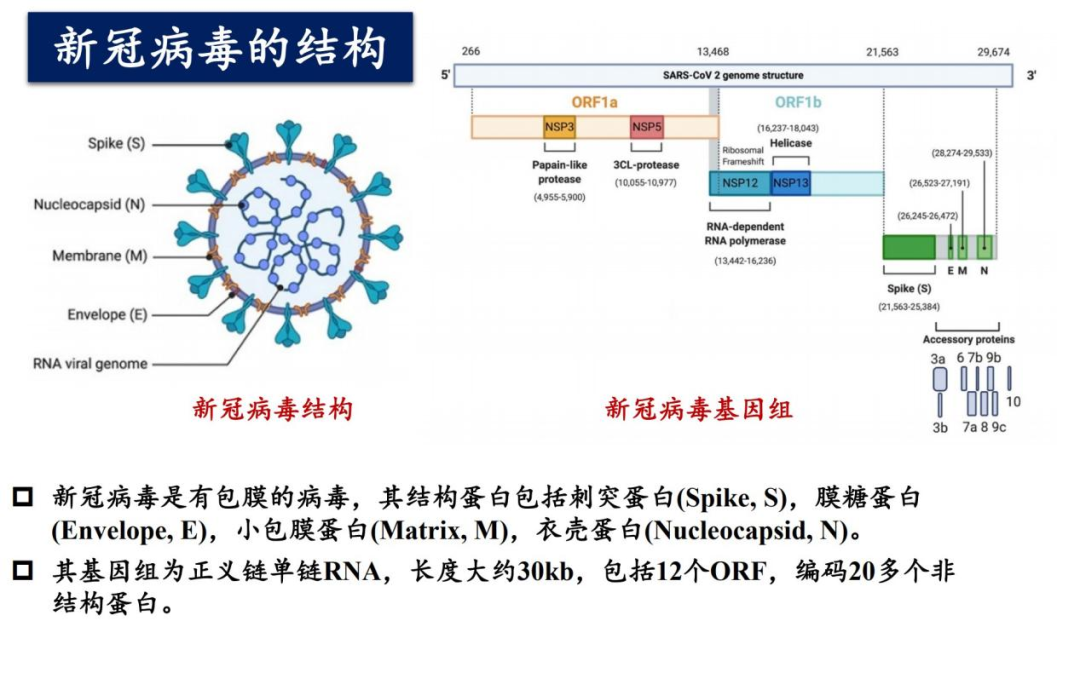
新冠病毒最早在中国武汉被发现,有关病毒的起源有各种各样的阴谋论。但从科学的角度来分析,越来越多的动物被证实可以携带和传播新冠病毒。在蝙蝠和穿山甲身上分离到的冠状病毒和新冠病毒的受体结合区域高度类似,且具有进化上的时序性;而对这些冠状病毒刺突蛋白S1和S2亚单位切割位点的分析也表明,新冠病毒特异性的PRRA插入突变,在云南菊头蝠冠状病毒上也天然存在。这些证据表明,蝙蝠和穿山甲很可能是新冠病毒的自然界的动物宿主。
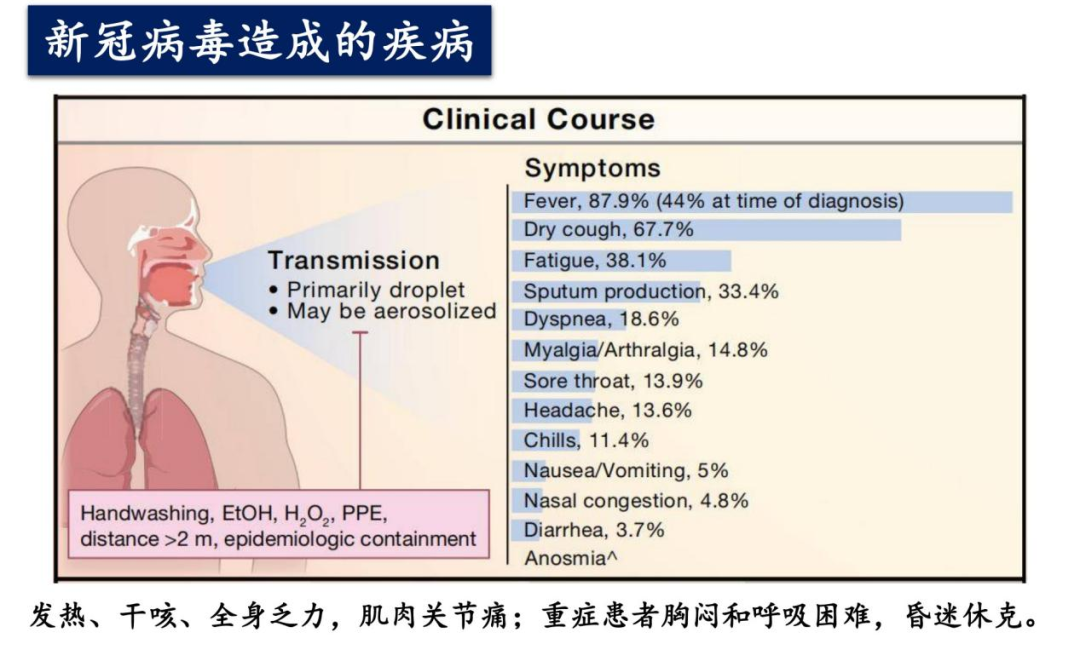
新冠病毒属于典型的呼吸道传播病毒,其主要依靠直接接触时的空气飞沫,以及新冠患者呼吸时产生的气溶胶的传播。同时有证据表明,新冠病毒很可能还存在着从物到人的接触传播。由于我国的动态清零的新冠防控策略,人与人接触的传播链条可以被精确回溯。在我国发生的多起疑似新冠病毒“物传人”的疫情中,当地的其它病例已经动态清零,感染者和已有病例没有接触;遗传溯源发现这些毒株和当地流行的病毒有着显著性差异,却和境外毒株高度相似。同时,从冷链运输的物品上也分离出了活的新冠病毒。这些流行病学证据指向,新冠病毒极有可能存在由物传播到人的传播途径。

新冠病毒是RNA病毒,其基因组缺乏稳定的复制纠错机制,病毒发生突变的频率很高。伴随着病毒的流行,病毒和宿主间相互适应,一些有利于病毒感染和传播的突变会被自然选择筛选出来。在这里需要指出的是,对于病毒来说,其生存策略是为了维持自身在自然界的延续,杀死宿主对病毒并没有好处。如果给病毒足够长的时间和宿主协同进化,最终它们会达到一种平衡。从旁观者的角度来看,病毒的对宿主的致病能力会慢慢变弱,但传播能力在不断变强,当前新冠病毒的进化趋势就符合这一特征。研究病毒的遗传进化,寻找并鉴定其中的重要突变,有着极其重要的基础科研和转化应用意义。它可以帮助我们理解病毒的致病机理,分析病毒的进化规律,预警病毒潜在的爆发和流行;也可以帮助我们改进各类病毒基因工程学工具和疫苗策略,提供新的抗体和药物的靶点。因此,我们的科学问题就是,新冠病毒是如何不断进化突变,来维系自身在宿主间的高效传播?哪些重要的突变位点可以增强病毒的感染和传播。
新冠病毒流行至今,产生了很多不同的变种病毒,其中最有代表性的变种病毒包括新冠病毒Alpha株,最早在英国被鉴定;Beta株,最早在南非被发现;Delta株在印度起源,并扩散至全球;Gamma株,在南美洲巴西当地广泛流行。以及最新出现的Omicron株,2021年底于南非出现,并迅速席卷全球。当我们对不同毒株的病毒序列进行生物信息学比对,可以发现很多不同的氨基酸突变,但并不是所有的突变都会具有生物学功能。在生物的遗传进化中,由于奠基者效应等遗传漂变现象,很多对病毒没有作用,甚至有害的突变也会在自然界中出现,甚至达到相当高的基因频率。我们必须通过生物学实验,对这些突变位点进行逐一验证,才能了解它们的生物学功能。
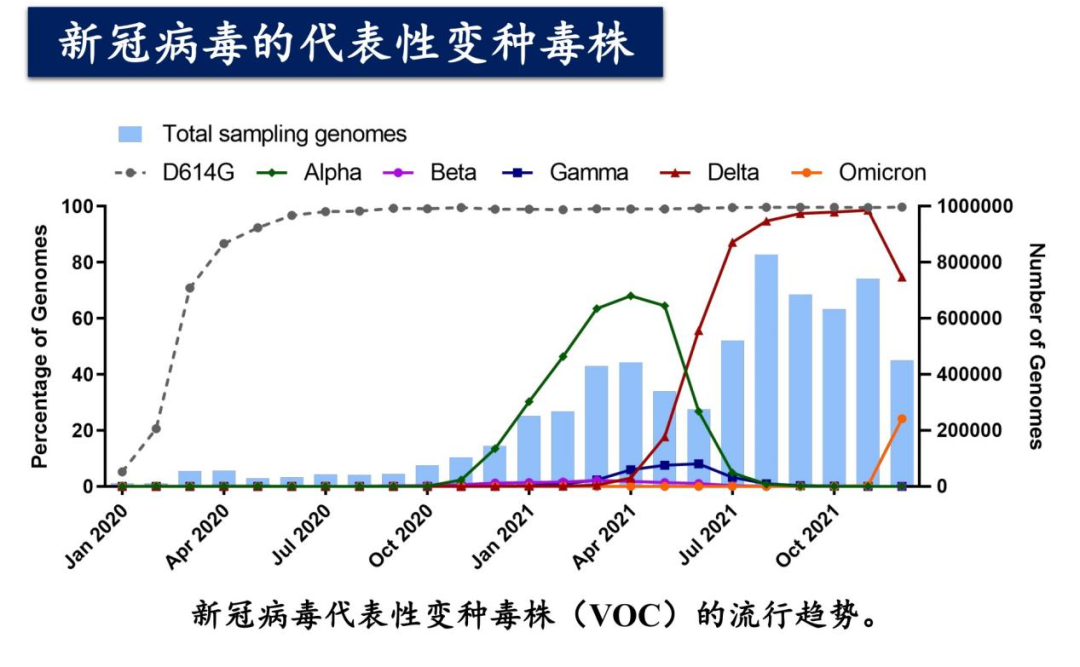
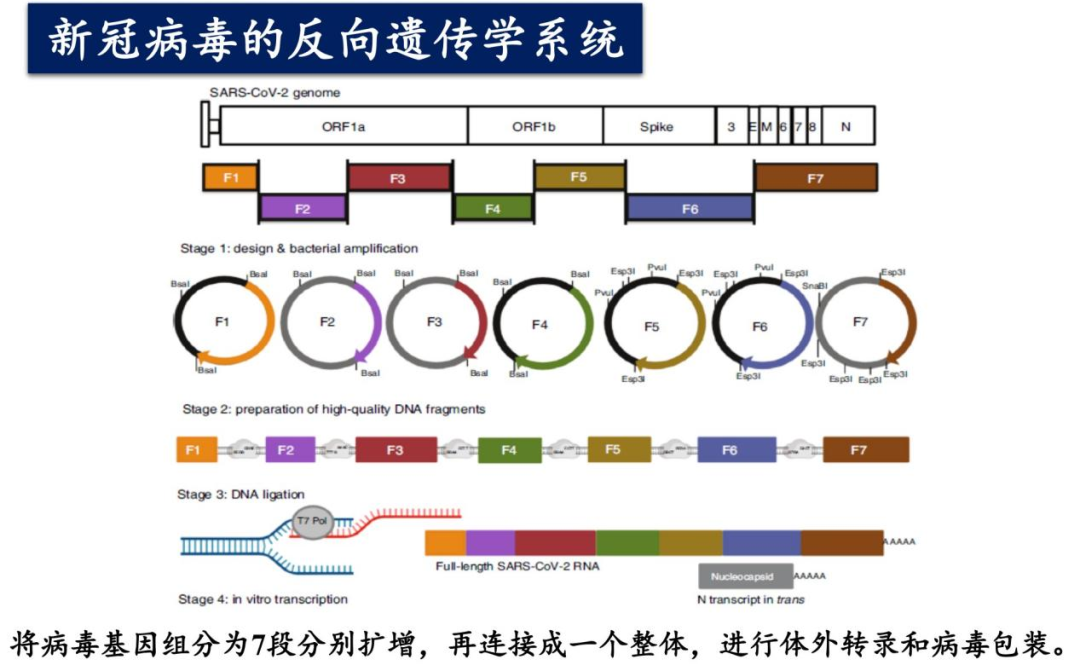
图1
之前的介绍中已经提到,新冠病毒表面的spike刺突蛋白,是介导病毒在细胞上吸附和侵入的重要蛋白;当新冠病毒传播到一个新的宿主时,快速的识别结合,并侵入靶细胞是建立早期感染的关键步骤。同时,刺突蛋白也是新冠病毒表面最主要的抗原,人体在新冠疫苗接种或者被病毒感染后,产生的抗体基本都是针对刺突蛋白发挥作用。新冠病毒刺突蛋白发生的突变,最容易影响新冠病毒感染和传播能力,也是病毒逃逸宿主抗血清识别的关键。因此,我的研究主要是围绕新冠病毒的刺突蛋白展开。
在新冠病毒2020年开始流行后不久,流行病学的数据分析就发现,新冠病毒刺突蛋白的第614位氨基酸出现了从天冬氨酸D到甘氨酸G的突变,这一突变的在自然界中的基因频率飞速上升,表明该突变极有可能影响病毒的感染。我们使用了人肺部上皮细胞组织模型,通过竞争实验对这一突变的功能进行验证。竞争实验,就是模拟病毒在自然界中真实进化角逐的过程,将不同突变病毒置入同样的感染系统中,通过检测不同变种病毒数量的比例来判断哪一种突变病毒在进化中占据优势。我们的实验发现,新冠病毒刺突蛋白D614G突变会非常显著的提高病毒在人肺部上皮细胞中的感染和复制能力。
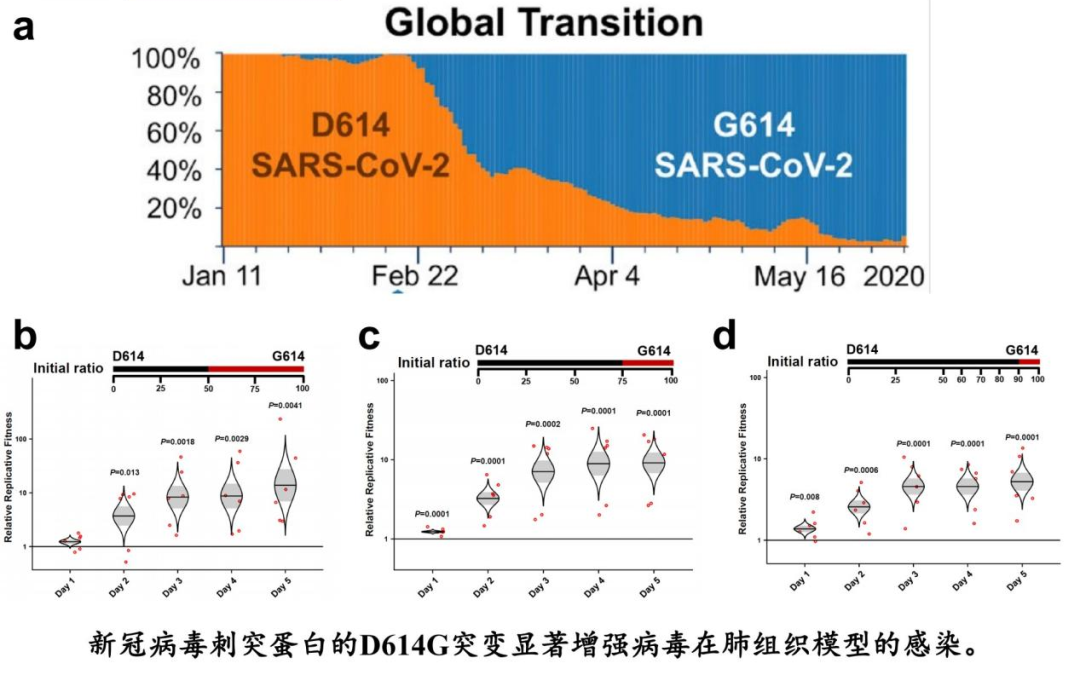
同时,在仓鼠等动物模型上的的研究结果也证明了,D614G病毒在动物的鼻腔和上呼吸道中具有更强的复制能力,从而促进病毒的传播和扩散。目前新出现的各类新冠病毒变种都具有D614G位点突变,G614的基因频率已经达到了接近100%。这项研究在当时前瞻性的预测了,D614G突变在病毒遗传进化上的优越性,并解释了其促进传播的机制。
在之后的另外一项研究中,我们发现2020年底英国出现的新冠病毒的alpha毒株,其致病和传播能力都要强于原始的毒株。我们通过反向遗传学手段,将alpha毒株上的8个标志性氨基酸位点逐一突变,再使用仓鼠传播模型,进行竞争实验去评估突变病毒传播能力的变化。我们将突变病毒和野生型病毒混合,通过鼻腔接种让供体仓鼠感染;在病毒感染供体仓鼠一天后,再将干净的受体仓鼠和感染的供体仓鼠共同饲养8个小时,让病毒自然的在动物间进行传播。 随后,我们对供体和受体仓鼠的鼻腔洗涤液,气管等组织中的突变病毒和野生病毒的比例进行检测。结果表明只有具有刺突蛋白N501Y突变的病毒,在仓鼠的鼻腔和气管中均保持显著的竞争优势。
随后的机制实验表明,刺突蛋白N501Y突变,会大幅度增强病毒和其重要细胞表面受体ACE2的结合,从而促进病毒对细胞的早期感染,加速病毒在自然界中的传播和扩散。这项研究鉴定并证明了新冠病毒刺突蛋白N501Y突变对病毒流行的重要促进作用,并解释了其分子机制。最近Omicron变异株疯狂流行,当Omicron突变株首次出现时,我们发现其携带了N501Y突变,就预测该毒株传播和扩散的能力会数倍于其它突变株。尽管全球各国政府第一时间将针对Omicron的戒备级别提升到最高,但是由于Omicron病毒在南非发现的太晚,已经在欧美隐性扩散开来,Omicron变体在全球的大流行不可避免。
除了我们重点研究的刺突蛋白D614G和N501Y突变以外,刺突蛋白上其它的氨基酸突变也在病毒的感染和免疫逃逸中发挥重要的作用。图2表格汇总了其中一些重要的氨基酸突变,可以看到,其中的相当一部分免疫逃逸相关的突变都出现在了最新的Omicron突变株上,这也是Omicron株能够显著性逃逸宿主抗血清和大量中和性单克隆抗体识别的关键。

图2
图文来源 | 刘洋课题组