基孔肯雅病毒的前世今生(上)|湾语前沿
2025年7月,一场突如其来的病毒袭击打破了岭南盛夏的宁静。名为“基孔肯雅”的病毒经由境外输入广东省佛山市顺德区后迅速扩散。截至7月26日,疫情已波及全省12个城市,累计报告感染病例近5000例。这场突发公共卫生事件引发广泛关注,也让许多人对这个陌生而拗口的病毒产生疑问:基孔肯雅病毒为何突然现身中国?它是如何在人群中传播并引发疾病的?本文将从病毒的视角出发,探寻基孔肯雅病毒的起源与进化,解析其传播路径、入侵机制与致病过程,带领读者全面了解这一病毒的“前世今生”。
起源与进化:源自非洲的“关节痛病毒”
基孔肯雅病毒(Chikungunya virus,简称CHIKV)是一种通过蚊虫传播的病毒,最早于1952年在非洲坦桑尼亚被发现。“基孔肯雅”一词源自当地语言,意为“蜷曲成一团”,形象地描述了患者因剧烈关节疼痛而弯腰屈身的典型姿态。从分类上看,基孔肯雅病毒属于披膜病毒科甲病毒属,与我们熟知的黄病毒科的登革病毒和寨卡病毒是“近亲”,三者均通过伊蚊叮咬传播,具有相似的基因结构和传播方式。从病毒结构来看,它是一种由单链RNA病毒,其基因组长约11.8 kb。病毒基因编码两类蛋白:非结构蛋白(nsP1-nsP4)用于病毒复制和免疫调控;结构蛋白则包括衣壳蛋白C和病毒表面的刺突蛋白(E1、E2等)。其中E1和E2蛋白像病毒感染细胞的“钥匙”,负责病毒进入宿主细胞。
基孔肯雅病毒在进化过程中形成了三个主要分支:东/中/南非型(ECSA型)、西非型和亚洲型。基孔肯雅病毒最初在非洲和东南亚的丛林地区流行,随着病毒对媒介和宿主的适应性进化,2004年,ECSA型病毒在包膜E1蛋白第226位发生了关键突变——丙氨酸(A)被替换为缬氨酸(V),即“E1-A226V突变”。这一突变显著增强了病毒感染白纹伊蚊(亚洲虎蚊)的能力,使其摆脱了对埃及伊蚊的依赖,并借助白纹伊蚊的耐寒特性,大幅拓展了在高纬度地区的传播范围[1]。凭借这一关键突变,2005年,基孔肯雅病毒在印度洋群岛迅速传播,累计感染数百万人。此后,病毒搭乘蚊子“航班”,加速扩散至欧洲、美洲等多个地区。截至2024年底,世界卫生组织统计显示,全球已有119个国家和地区报告基孔肯雅疫情,每年累计病例超过50万。我国华南地区气候温暖湿润,蚊虫种类丰富,为蚊媒病毒传播提供了有利条件。本次广东省的基孔肯雅疫情由境外输入病例引发,随后在本地迅速扩散并形成大规模传播。
传播和扩散:病毒在蚊和人间的“穿行之旅”
基孔肯雅病毒最早在非洲和东南亚的丛林中流行,在非人灵长类动物与蚊子之间传播,形成“丛林循环”;其中灵长类动物是关键的病毒储存宿主。一旦带毒蚊虫叮咬人类,病毒便可跳出丛林生态系统,在人类与蚊子之间建立“城市循环”。与流感等可经空气传播的病毒不同,基孔肯雅病毒并不在人与人之间直接传播,而是高度依赖蚊虫叮咬来传播扩散,在“人-蚊”之间完成其复杂而精妙的生命周期[2]。
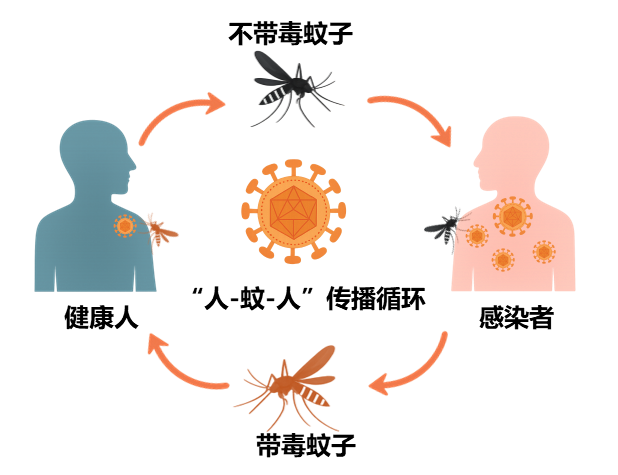
当带毒蚊虫叮咬人类时,病毒会随唾液进入皮下组织,迅速感染局部的成纤维细胞、肌肉细胞等,并在体内快速复制。随后,病毒进入血液循环,引发病毒血症,并进一步扩散至关节滑膜、骨骼肌等组织,在这些部位继续大量复制,诱发机体强烈的免疫反应。免疫系统释放的大量炎症因子,导致高热、皮疹以及剧烈的关节疼痛等典型症状。急性感染期一般持续1至2周,但部分患者可能发展为慢性关节炎,关节疼痛可持续数月甚至更久,严重影响生活质量。
当蚊子叮咬处于病毒血症期的患者时,病毒会随血液进入蚊虫的中肠,并在其中迅速复制扩增。随后,病毒突破中肠屏障,进入蚊体的血淋巴系统,并进一步扩散至唾液腺。当病毒在唾液腺中大量复制后,蚊子便具备了传播病毒的能力。蚊虫自感染病毒到具备传播能力的这段时间被称为“外潜伏期”,通常持续4至8天。此后,当蚊虫再次叮咬健康人时,唾液中的病毒便被“注射”入宿主体内,完成一轮传播。由于蚊子可多次叮咬不同个体,实际上成为病毒的“流动针头”,使得病毒在人群中持续扩散。尤其在温暖湿润的环境中,蚊虫繁殖迅速,进一步加快病毒的传播速度与范围。因此,蚊虫不仅是传播所必需的媒介,更是决定病毒能否在人群中引发大规模流行的关键因素。
除了通过蚊虫叮咬传播给人类(即水平传播)外,基孔肯雅病毒还可在蚊体内通过一种特殊机制传递给后代(即垂直传播):病毒能够穿越卵巢屏障进入卵细胞,使新孵化的幼蚊先天携带病毒。虽然这一传播方式的发生率较低(约0.5%~3%),但它为病毒在干旱或低温等不利环境中实现长期存续提供了可能,使其能够在自然界中“隐匿”存留,等待适宜条件再次传播流行。
参考文献:
[1] TSETSARKIN K A, VANLANDINGHAM D L, MCGEE C E, et al. A single mutation in chikungunya virus affects vector specificity and epidemic potential [J]. PLoS Pathog, 2007, 3(12): e201.
[2] LYARUU L. Chikungunya Virus Transmission [M]//ENGOHANG-NDONG J. Chikungunya Virus - A Growing Global Public Health Threat. Rijeka; IntechOpen. 2022.
PI简介:

刘 洋
刘洋博士,长期致力于病毒的遗传进化和致病机理研究,其研究鉴定新冠病毒、登革病毒和寨卡病毒上的多个影响病毒感染和传播的重要氨基酸突变,揭示了这些病毒在自然界中的遗传进化规律,为这些病毒疫情的防控提供了科学指导。刘洋博士在新冠疫情发生后,搭建了多种研究新冠病毒的重要反向遗传学平台,并在世界上首次评估了新冠疫苗对多种突变新冠病毒中和能力的变化,为新冠疫苗后续接种策略的改进提供了重要依据。
刘洋博士于2022年加入深圳湾实验室传染病所,任特聘研究员,获得清华大学/西湖大学/华南理工大学/中山大学的博士生/硕士生导师资格,并担任广东省感染与免疫重点实验室副主任,中华医学会病毒学分会青年专委会委员等职位。其归国后获得了2021年中华医学科技奖二等奖(第3完成人),2022年教育部科学技术奖一等奖(第4完成人);主持2022年国家优秀青年科学基金项目(海外)、国自然面上、国自然专项和国家重点研发计划子课题负责人等科研项目。其研究成果以第一作者/通讯作者(含共一/共通讯)的身份发表于Nature, New Engl. J. Med., Cell, Nat. Med., Nat. Microbio, Nat. Commun.等国际知名期刊,累计影响因子达600,所有文章引用次数超4500次。
课题组主要着眼于重要人类病毒的遗传进化和致病机理研究,新型病毒工具和抗病毒策略的研发。将运用反向遗传学、病毒学、免疫学,影像学、生物信息学和各种组学研究手段,寻找病毒上和宿主中影响病毒感染和传播的重要突变和关键因子,阐述其发挥作用的分子机制;并以这些病毒突变和宿主因子为靶点,研发新型抗病毒策略和治疗手段。同时,课题组开发各种新型病毒载体工具,应用于病毒学领域的基础研究,药物、抗体和疫苗的筛选及评估,药物的递送和疾病的治疗,为各种新发突发病毒传染病的防控提供科技支撑。
来源 | 刘洋课题组